photo credit: ilovebutter via photopin cc
永野数学塾の「虎の巻」を公開する「語呂合わせと徹底整理で攻略する高校無機化学」シリーズ4回目の今日は、14族の炭素、ケイ素篇です。
このシリーズをまとめたものは↓
まずは炭素から!
炭素C
炭素は同素体(同じ元素からなる単体で性質の異なる物質)をもちます。
※ 炭素の化合物は5千万種類以上もあって、有機化合物の世界を作っている。
炭素の同素体
- 電気を通さない。
- 非常に硬く融点が高い。
- 立体網目構造。
- 電気や熱を通す※。
- 平面層状構造。
※ ダイヤモンドは4個の価電子が全て結合に使われ、上の図のような立体網目構造を作っているために非常に固くまた融点も高い。一方の黒鉛では3個の価電子が結合に使われ平面層構造を作っていて、1つの価電子が余っている。この余った価電子が結晶の平面内を金属の自由電子の様に動くことができるので黒鉛は電気を通す。
無定形炭素
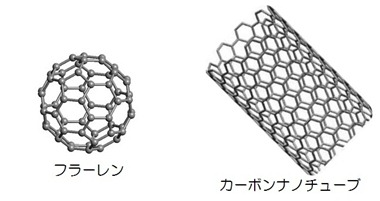
炭素の同素体にはダイヤモンド、黒鉛、無定形炭素の他にも20世紀末に以下の2つの同素体が発見されました。これらの同素体についはこれからの研究が期待されています。
- 球状炭素分子。
炭素は化合物も重要です!
炭素の化合物
CO(一酸化炭素)
- 無色・無臭。
- 猛毒。
- 中性。水には不溶。
- 還元性がある。
- 炭素の不完全燃焼で生じる
CO2(二酸化炭素)
- 無色・無臭。
- 水に少し溶けて弱酸性。
CO2 + H2O → 2H+ + CO32-
Ca(OH)2 + CO2 → CaCO3↓ + H2O
ケイ素Siとケイ素の化合物
Si(ケイ素)
- ダイヤモンドと同じ構造をもち、硬く、融点が高い。
- 半導体の材料。
- 単体は天然に存在せず、二酸化ケイ素をコークス(C)で還元することで得られる。
SiO2 + 2C → Si + 2CO
SiO2(二酸化ケイ素)
- シリカゲルの原料。
- 水を加えて加熱すると水ガラス=粘性の大きな液体になる。
SiO2・nH2O(シリカゲル)[nは0に近い任意の数。水分約5%]
- 乾燥剤※1。
- ケイ酸ナトリウムから得られたケイ酸(H2SiO3)※2を加熱・乾燥することで得られる。
Na2SiO3 + 2HCl → 2NaCl + H2SiO3
(弱酸の塩 + 強酸 → 強酸の塩 + 弱酸)
※1 シリカゲルは多数の小さな穴のあいた構造をもち、表面にある-OH基によって水分子を捕まえる。
 シリカゲルの構造
シリカゲルの構造
※2 ケイ酸(H2SiO3)は非常に弱い酸。
セラミックス
ケイ砂(SiO2)、ケイ酸塩(ケイ酸イオンSiO32-と金属イオンが結合した化合物)を含んだ粘土と石灰石などの無機物を高温処理してできる固体をセラミックスという。
代表的なセラミックス … 陶磁器、ガラス、セメントなど

photo credit: H is for Home via photopin cc
セラミックスを作る工業をケイ酸塩工業(窯(よう)業)という。